En este sitio tendrás la oportunidad de actualizar tus conocimientos de enfermería,aclarar dudas sobre temas diversos y intercambiar información sobre nuestra profesión.
martes, 22 de marzo de 2011
Actualizaciones en enfermería: el A H1N1 virus mortal
Actualizaciones en enfermería: el A H1N1 virus mortal: "Colegas hay un repunte de A H1N1 en Venezuela específicamente en el estado merida. En lo que va del año, son 3 l..."
Actualizaciones en enfermería: hipertensión arterial sistemica
Actualizaciones en enfermería: hipertensión arterial sistemica: "Definición La hipertensión arterial sistémica (HTAS) es una enfermedad crónica, controlable de etiología multifactorial, que se caracteriz..."
hipertensión arterial sistemica
Definición
La hipertensión arterial sistémica (HTAS) es una enfermedad crónica, controlable de etiología multifactorial, que se caracteriza por un aumento sostenido en las cifras de la presión arterial sistólica (PS) por arriba de 140 mmHg , y/o de la presión arterial diastólica (PD) igual o mayor a 90 mmHg
Importancia de la hipertensión arterial sistemica
La hipertensión arterial sistémica es un importante problema de salud pública, no sólo por su alta incidencia y prevalencia, sino por su estrecha asociación con el desarrollo de las enfermedades cardiovasculares y cerebrovasculares.La prevalencia de HAS en México es de 30.7% en adultos mayores de 20 años, sin embargo 2 de cada 3 hipertensos desconoce su enfermedad,de éstos poco más de la mitad reciben tratamiento antihipertensivo y sólo el 14.6% logran su control tensional.
Dependiendo de los factores asociados a su desarrollo, la HTAS puede clasificarse como esencial
(primaria) y secundaria.
Las primarias (esenciales) representan entre el 90-95% de los casos y son de etiologia multifactorial; están relacionadas con:
Antecedentes hereditarios de hipertensión
- Sobrepeso y obesidad.
- Sedentarismo.
- Estrés mental.
- Hábitos alimenticios: consumo excesivo de alimentos ricos en sodio y bajos en potasio, pobre ingesta de verduras y frutas.
- Abuso en el consumo de alcohol y drogas.
- Tabaquismo.
Otros factores de riesgo que precipitan la aparición
La HTAS en individuos mayores de 30 años son:
- Uso de medicamentos (vasoconstrictores, antihistamínicos, esteroides, AINES).
- Diabetes mellitus (DM).
- Síndrome cardiometabólico.
Únicamente son secundarias el 5-10% de los casos, y están asociadas a las siguientes causas:
- Apnea del sueño.
- Insuficiencia renal crónica.
- Aldosteronismo primario.
- Enfermedad renovascular.
- Feocromocitoma.
- Coartación de la aorta.
- Enfermedad tiroidea o paratiroidea.
- Terapia con esteroides o síndrome de Cushing.
Diagnostico de la Hipertensión arterial
Posiblemente el primer experimento para medir la presión arterial fue
realizado por el obispo de Teddinghan, Stephen Hales, que comunicó
en 1733 al Colegio Real de Médicos sus observaciones realizadas en
un caballo al que canuló la arteria carótida, notando que la sangre era capaz
de subir 270 centímetros por encima del corazón. Así empezó todo, pero no
sabemos lo que pasó con el caballo que, posiblemente, encabeza la lista
de las víctimas de la iatrogenia (por lo menos de tipo “veterinario”) por la
medición inadecuada de la presión arterial.
Hasta fines del siglo XIX las mediciones de la tensión arterial se realizaban con complicados instrumentos de laboratorio y solo en este tipo de ambiente experimental.
En 1896 en la Gaceta Médica de Torino apareció el artículo de “Scipione
Riva-Ricci”, sobre las características de un nuevo aparato para medir la
presión arterial: el esfigmomanómetro de mercurio. Este descubrimiento
simple permitió una gran mejoría en el conocimiento de la hipertensión arterial y posibilitó la medición de la presión en un escenario más amplio y lo
introdujo en la práctica clínica diaria. La técnica fue perfeccionada gracias a la observación de Nikolai Sergeyevich Korotkoff en 1905, quien, al aplicar el fonendoscopio sobre la arteria colapsada y luego liberada, describió los ruidos que llevan su nombre y de esta
manera se introdujo el método auscultatorio utilizado hasta nuestros días.
En el nuevo siglo los estudios experimentales y las observaciones clínicas
permitieron conocer las regulaciones mecánicas de la presión arterial en
condiciones fisiológicas y patológicas.
En los años cincuenta algunos médicos creían que la presión sanguínea elevada era necesaria para proveer adecuado flujo a los órganos vitales,conforme
la persona envejecía.
Uno de los estudios iniciales que destaco el riesgo de
presión no tratada fue publicado en 1955; de los 500 pacientes evaluados y seguidos desde el diagnóstico de la HTA hasta la muerte, con un seguimiento máximo de 44 años, aproximadamente el 50% desarrolló falla cardíaca y el 12% presentó apoplejía; el daño renal se encontró en 42% de los casos y la falla renal crónica en el 18%. El daño de órganos blancos fue acompañado de un aumento significativo de la mortalidad, con una sobre vida media entre 1 y 8 años después de iniciada la hipertensión. En forma paralela las estadísticas de las compañías de seguros estadounidenses, resaltaban que las expectativas de vida disminuían cuando la presión arterial aumentaba. Se inicia así la concepción de la hipertensión arterial como factor de riesgo cardiovascular.El manejo de la hipertensión ha sufrido profundos cambios desde los años 40 del siglo pasado, cuando muchos médicos aún no estaban convencidos de que una elevación de la presión sanguínea incrementaba grandemente el riesgo.El tratamiento de la hipertensión en aquellas épocas era primitivo y consistía en una dieta muy rígida baja en sodio que pocos pacientes podían seguir, cirugías mutilativas (simpatectomía o adrenalectomía bilateral), y unas pocas medicaciones cuyos efectos tóxicos impedían su utilización amplia. Los estudios a finales de los años 40 establecieron que si la presión lograba ser reducida en pacientes con la presentación maligna y además era mantenida en un nivel bajo, se evitarían muchos accidentes cerebrovasculares y episodios de falla cardíaca, también se incrementaba la sobrevida. Los médicos empezaron a tratar pacientes con hipertensión menos severa en los años 60 a 80, en la medida que los datos de estudios clínicos confirmaron
que aun elevaciones de la tensión arterial por encima de un límite arbitrario de 140/90 mmHg incrementaban el riesgo cardiovascular, y que disminuyéndola por debajo de estos niveles disminuirían las complicaciones. Con la acumulación de más información se hizo aparente que los beneficios de tratar grados menos severos de hipertensión sobrepasaban los riesgos, tanto en sujetos jóvenes como viejos. La información más reciente tiene .que ver con los beneficios claros de tratar pacientes de edad avanzada con hipertensión sistólica aislada.La disminución de las enfermedades cardiovasculares es a lo lejos el mayor logro de la medicina en la última mitad del siglo XX. Podemos decir que el tratamiento de la HTA es la única intervención médica que ha dejado una huella clara en las tendencias de mortalidad.
.
Presentación clínica y técnica de medición
No hay síntomas específicos que sugieran hipertensión arterial. Ocasionalmente los pacientes refieren cefalea occipital o mareos, síntomas completamente irrelevantes y no específicos.La hipertensión solo puede ser identificada después de tomada con los equipos convencionales. Hay tres razones para explicar su variación: métodos inadecuados de toma, variabilidad inherente por ritmos circadianos y tendencia al incremento de la presión arterial en presencia del médico (el llamado efecto de “bata blanca”). En la práctica clínica el “patrón de oro” es la medición hecha con el esfigmomanómetro de mercurio con la técnica auscultatorio de Korotkoff. Uno de los problemas actuales es que el mercurio está siendo prohibido en ciertos países y aun no hay certeza de qué lo va a reemplazar, aunque los equipos aneroides parecen ser los indicados. Para los propósitos clínicos debe establecerse un umbral por encima del cual los pacientes deben ser tratados, aunque no hay otra justificación para esta separación tan rígida.
Hasta el momento los valores de la presión en el consultorio son tomados como los promedios o “verdaderos”, para definir una estrategia terapéutica, sin embargo la situación empieza a modificarse. Los avances recientes en la técnicas de medición de la presión arterial, particularmente el monitoreo ambulatorio, han comenzado a proveer la oportunidad de examinar el rol patológico de otras mediciones, como las anormalidades en el ritmo diurno y la variabilidad a corto plazo.
Método auscultatorio.
No se ha modificado ni mejorado en 100 años. El método de Koroktoff tiende a dar valores de presión sistólica menores que la intra arterial y valores de presión diastólica que son mayores que con la técnica invasiva. La recomendación es tomar el inicio de ruidos como la presión arterial sistólica y la fase 2 (desaparición del ruido) como la presión arterial diastólica. La mayoría de los estudios clínicos a gran escala que han evaluado los beneficios de tratar la HTA han usado la fase cinco como dato de la PAD.
.Técnica oscilométrica.
Durante la toma de la presión arterial convencional con tensiómetro de mercurio o manómetro siempre se observan oscilaciones en el nivel del mercurio o la aguja cuando se inicia el desinflado del manguito. La primera oscilación ocurre con la aparición de la presión sistólica y continúa aún por debajo de la
presión diastólica. Esta anotación clínica se trasladó al terreno experimental encontrando que cuando se presenta la máxima oscilación, el nivel de presión que se registra en ese momento corresponde a la presión arterial media (PAM). Después de obtenido este dato y conociendo la PAS, con un algoritmo derivado empíricamente, las máquinas de toma de presión logran dar todos los datos que necesitamos: PAS, PAM y PAD.
El manguito de estos equipos tiene sensibilidad para detectar estas oscilaciones de un modo muy exacto.
Una ventaja del método es que no necesita trasductor y se afecta menos por el ruido externo, pero no funcionan bien durante el ejercicio físico. Es la técnica usada en monitores ambulatorios, módulos de presión no invasiva de hospitales y equipos de monitoreo casero; tienen buena correlación con el método auscultatorio.
Técnica por ultrasonido
Hay un trasmisor y receptor sobre la arteria braquial. Más útil en niños e infantes.
Método del cojín en el dedo de Penaz
La pulsación arterial en el dedo es detectada por un fotopletismógrafo ubicado
debajo del cojín de presión. Las oscilaciones de la presión arterial lucen iguales a las ondas de presión intra arterial.
.
Aspectos técnicos
Hay varias fuentes de error, algunas de las más comunes son: Efecto de la postura: se recomienda que el paciente esté sentado, con los pies apoyados en el piso y la espalda con soporte. Si se toma en posición erecta afecta la presión diastólica en jóvenes. En los pacientes de edad o con sospecha de ortostatismo se recomienda realizar mediciones de pie después de tres minutos. Posición del miembro superior: por efecto de presión hidrostática, la PA es más alta si el brazo no se mantiene a la altura del corazón, apoyado en una mesa o en la mano del médico. Cada centímetro que el centro del manguito ocupe por
debajo del corazón implica un aumento de 0,8 mmHg, en la medición.
Hipertensión inducida por el inflado: en pacientes ocasionales puede subir transitoriamente, hasta 40 mmhg la cifra de presión arterial, por la aprehensión que produce el inflado del manguito. Debe diferenciarse de la HTA de bata blanca, porque esta precede la toma.
Tamaño del manguito: es crucial. Debe usarse un manguito que ocupe 2/3 del brazo y la longitud de la “vejiga” del manguito debe cubrir al menos el 80% de la circunferencia del brazo. El error más común es usar un manguito pequeño, lo que resulta en una sobreestimación de la presión. Desinflado: debe hacerse a una tasa de 2 mmHg por latido. Si se realiza rápido las lecturas, especialmente en pacientes bradicárdicos serán muy inadecuadas.
El efecto de la bata blanca: es una de las principales razones para el auge de las determinaciones de la presión arterial por fuera del consultorio. El mecanismo subyacente no está bien establecido pero puede incluir ansiedad, respuesta alerta hiperactiva o una respuesta condicionada. Se ve en mayor o menor grado en todos los hipertensos y es poco frecuente en normotensos.
.
La HTA de bata blanca
Define un grupo de pacientes que son hipertensos en el consultorio y normotensos por fuera de allí. Por más de cuarenta años se ha sabido que los niveles de tensión sanguínea tomados por el médico pueden ser hasta 30 mmHg más altos que los tomados en casa por el paciente, usando la misma técnica y postura. Los médicos obtienen también mediciones más altas que las enfermeras y los técnicos. Es importante clínicamente porque se considera una condición de bajo riesgo. Entre los pacientes diagnosticados como hipertensos leves se encuentra una prevalencia del 20%. Solo puede ser diagnosticada con el monitoreo ambulatorio de presión arterial y no debe rotularse el paciente como tal en la primera cita. Una vez diagnosticada la hipertensión de bata blanca el seguimiento debe ser cercano pues un porcentaje importante terminan siendo hipertensos reales.
domingo, 20 de marzo de 2011
La aspirina
Ácido acetilsalicílico
 | |
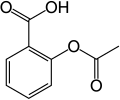 | |
Ácido acetilsalicílico | |
| Nombre (IUPAC) sistemático | |
| Ácido 2-(acetiloxi)-benzoico | |
| Identificadores | |
| Número CAS | 50-78-2 |
| Código ATC | B01AC06 |
| PubChem | 2244 |
| DrugBank | APRD00264 |
| ChEBI | 15365 |
| Datos químicos | |
| Fórmula | C6H4(OCOCH3)COOH |
| Peso mol. | 180,16 uma |
| Sinónimos | Ácido acetilsalicílico, Ácido o-acetilsalicílico, Acetilsalicilato, Ácido 2-acetoxibenzoico |
| Datos físicos | |
| Densidad | 1,40 g/cm³ |
| P. fusión | 138 °C (280 °F) |
| Punto de ebullición | 140 °C (284 °F) |
| Solubilidad enagua | 1 mg/mL (20 °C) |
| Farmacocinética | |
| Biodisponibilidad | Rápida y completa |
| Unión proteica | 99,6% |
| Metabolismo | hepático |
| Vida media | 300-650mg: 3,1-3,2 horas; Dosis 1 g:5 horas; Dosis 2 g:9 horas |
| Excreción | Renal |
| Consideraciones terapéuticas | |
| Cat. embarazo | C(AU) C(Estados Unidos) |
| Estado legal | Unscheduled(AU) |
| Vías adm. | Oral |
El ácido acetilsalicílico o AAS (C9H8O4), también conocido con el nombre deAspirina®, es un fármaco de la familia de los salicilatos, usado frecuentemente comoantiinflamatorio, analgésico, para el alivio del dolor leve y moderado, antipirético para reducir la fiebre y antiagregante plaquetario indicado para personas con alto riesgo de coagulación sanguínea,1 principalmente individuos que ya han tenido un infarto agudo de miocardio.2 3
Los efectos adversos de la aspirina son principalmente gastrointestinales, es decir, úlcera pépticas gástricas y sangrado estomacal. En pacientes menores de 14 años se ha dejado de usar la aspirina para el control de los síntomas de la gripe o de la varicela debido al elevado riesgo de contraer el síndrome de Reye.4
Contenido[ocultar] |
[editar]Historia

Salix alba, una de las 11especies del género Salixusadas en la antigüedad por sus propiedades antipiréticas.
La corteza de sauce blanco (Salix alba; "Salix", que significa "sauce" en latín, es el nombre del género) ha sido usada desde tiempo inmemorial para el alivio de la fiebre y del dolor, incluso por Hipócrates en el siglo V a. C.,5 los antiguos egipcios y los amerindios.6 Los efectos medicinales del sauce blanco continuaron siendo mencionados por observadores del pasado, incluyendo al farmacéutico Plinio el Viejo, al naturista Dioscórides y al filósofo Galeno.
En 1763 Edward Stone, reverendo de la Iglesia de Inglaterra, presentó un informe a Lord Macclesfield, quien presidía la Real Sociedad de Ciencia Inglesa, referente a estas propiedades terapéuticas de la corteza de sauce blanco destacando su efecto antipirético.7 Stone describió en su trabajo que había administrado el extracto en forma de té o cerveza a 50 pacientes febriles, aliviándoles elsíntoma.8 9 Investigaciones posteriores condujeron al principio activo de esta planta, que los científicos llamaronsalicilina, un análogo del ácido salicílico y del ácido acetilsalicílico.10
El principio activo fue aislado en 1828 por Johann Buchner, profesor de farmacia en la Universidad de Múnich; se trataba de una sustancia amarga y amarillenta extraída de agujas cristalinas que llamó salicina.5 Dos años antes, los italianos Brugnatelli y Fontana aislaron ese mismo extracto, pero en forma muy impura, y no lograron demostrar que la sustancia era la causante de los efectos farmacológicos del sauce blanco.10 En1829 un farmacéutico francés, Henri Leroux, improvisó un procedimiento de extracción del que obtuvo 30gramos de salicilina a partir de 1.5 kg de corteza. En 1838 Raffaele Piria, un químico italiano, trabajando en La Sorbona de París logró separar la salicina en azúcar y un componente aromático llamado salicilaldehído.8 A este último compuesto lo convirtió, por hidrólisis yoxidación, en cristales incoloros a los que puso por nombre ácido salicílico.5
Fue sintetizado por primera vez por Charles Frédéric Gerhardt en 1853 y luego en forma de sal por Hermann Kolbe en 1859.8 Hubo que esperar hasta 1897 para que el químico alemán Felix Hoffmann, de la casa Bayer, consiguiera sintetizar al ácido salicílico con gran pureza.11 Sus propiedades terapéuticas como analgésico y antiinflamatorio fueron descritas en 1899 por el farmacólogo alemán Heinrich Dreser, lo que permitió su comercialización.
Aspirina fue el nombre comercial acuñado por los laboratorios Bayer para el comprimido fabricado con esta sustancia,12 convirtiéndose en el primer fármaco del grupo de los antiinflamatorios no esteroideos, AINE. Posteriormente, en 1971, el farmacólogo británico John Robert Vane, entonces empleado del Royal College of Surgeons ("Colegio Real de Cirujanos") de Londres, pudo demostrar que el AAS suprime la producción deprostaglandinas y tromboxanos,13 lo que abrió la posibilidad de su uso en bajas dosis como antiagregante plaquetario, ampliando enormemente su campo comercial y compensando el hecho de que, en la actualidad, su uso como antiinflamatorio de elección haya sido desplazado por otros AINE más eficaces y seguros.14
Su trascendencia ha sido tanta que el nombre comercial terminó convirtiéndose en el nombre de uso cotidiano, de tal manera que en Estados Unidos aspirin pasó a ser el nombre genérico de la sustancia. Desde su comercialización se han consumido más de 350 billones de comprimidos y se estima que el consumo diario es de unos 100 millones de aspirinas.15 Consecuentemente, es uno de los fármacos más usados en el mundo, con un consumo estimado de 40.000 toneladas métricas anuales.16 En el año 2008, el 85% de la producción mundial de ácido acetilsalicílico se realiza en Langreo, España, en una planta química de la empresa multinacional Bayer.17 Desde allí se envía a diferentes partes del mundo donde se preparan los comprimidos y diferentes formas farmacéuticas en las que se vende Aspirina.
[editar]Descripción
El ácido salicílico o salicilato, producto metabólico de la aspirina, es un ácido orgánico simple con un pKa de 3,0. La aspirina, por su parte, tiene un pKa de 3,5 a 25 °C.18 Tanto la aspirina como el salicilato sódico son igualmente efectivos como antiinflamatorios, aunque la aspirina tiende a ser más eficaz como analgésico.14
La makesia es la producción del un ácido acetilsalicílico, se protona el oxígeno para obtener un electrófilo más fuerte.
La reacción química de la síntesis de la aspirina se considera una esterificación. El ácido salicílico es tratado con anhídrido acético, un compuesto derivado de un ácido, lo que hace que el grupo alcohol del salicilato se convierta en un grupo acetilo (salicilato-OH → salicilato-OCOCH3). Este proceso produce aspirina y ácido acético, el cual se considera un subproducto de la reacción.19 La producción de ácido acético es la razón por la que la aspirina con frecuencia huele como a vinagre.20
Como catalizador casi siempre se usan pequeñas cantidades de ácido sulfúrico y ocasionalmente ácido fosfórico. El método es una de las reacciones más usadas en los laboratorios de química en universidades de pregrado.21
[editar]Farmacocinética
[editar]Vías de administración (formas de uso)
El ácido acetilsalicílico se administra principalmente por vía oral, aunque también existe para usorectal y como terapia intravenosa. Los comprimidos de aspirina para administración oral sehidrolizan con facilidad cuando se ven expuestos al agua o aire húmedo, de modo que deben permanecer almacenados en sus envoltorios hasta el momento de su administración. La aspirina que se ha hidrolizado así despide un olor a vinagre (en realidad es ácido acético) y no debe ingerirse. La aspirina también viene en preparados masticables para adultos. Los preparados efervescentes y saborizados son aptos para quienes prefieran la administración líquida del medicamento.22 Es mayor la probabilidad de problemas severos del estómago con la aspirina que no tiene recubrimiento entérico.23
[editar]Absorción
La aspirina tiene muy escasa solubilidad en condiciones de pH bajo, como ocurre en elestómago, hecho que puede retardar la absorción de grandes dosis del medicamento unas 8-24 horas. Todos los salicilatos, incluyendo la aspirina, se absorben rápidamente por el tracto digestivo a la altura del duodeno y del intestino delgado, alcanzando la concentración máxima en el plasma sanguíneo al cabo de 1 a 2 horas.24 Por ser un ácido débil, muy poco queda remanente en forma ionizada en el estómago después de la administración oral del ácido salicílico. Debido a su baja solubilidad, la aspirina se absorbe muy lentamente en casos de sobredosis, haciendo que las concentraciones plasmáticas aumenten de manera continua hasta 24 horas después de la ingesta.2526 27 La biodisponibilidad es muy elevada, aunque la absorción tiende a ser afectada por el contenido y el pH del estómago.
[editar]Distribución
La unión del salicilato a las proteínas plasmáticas es muy elevada, superior al 99%, y de dinámica lineal.14 La saturación de los sitios de unión en las proteínas plasmáticas conduce a una mayor concentración de salicilatos libres, aumentando el riesgo de toxicidad. Presenta una amplia distribución tisular, atravesando las barreras hematoencefálica y placentaria. La vida media sérica es de aproximadamente 15 minutos. El volumen de distribución del ácido salicílico en el cuerpo es de 0,1–0,2 l/kg. Los estados de acidosis tienden a incrementar el volumen de distribución porque facilitan la penetración de los sacililatos a los tejidos.27
[editar]Metabolismo
La aspirina se hidroliza parcialmente a ácido salicílico durante el primer paso a través del hígado. Este metabolismo hepático está sujeto a mecanismos de saturación, por lo que al superarse el umbral, las concentraciones de la aspirina aumentan de manera desproporcionada en el organismo. También es hidrolizada a ácido acético y salicilato por esterasas en los tejidos y la sangre.
[editar]Excreción
La excreción se realiza a través de la orina y en mínimas cantidades por las heces. A medida que la cantidad de aspirina administrada aumenta, la vida media de eliminación de su metabolito, el ácido salicílico, se incrementa desde 3-5 horas (dosis de 600 mg cada día) hasta 12-16 horas (dosis mayores de 3,6 g cada día).14
La alcalinización de la orina aumenta la velocidad de excreción del ácido salicílico libre y sus conjugados hidrosolubles.
[editar]Farmacodinámica
[editar]Mecanismo de acción

Estructura de una molécula de COX-2inactivada por la Aspirina. En el sitio de acción de cada uno de los monómeros de la COX-2, la aspirina (la molécula gris más pequeña) ha acetilado a la serina de la posición 530. También en la imagen se ve elcofactor hemo con un átomo de hierro (la molécula gris con el hierro de color marrón).
Los mecanismos biológicos para la producción de la inflamación, dolor o fiebre son muy similares. En ellos intervienen una serie de sustancias que tienen un final común. En la zona de la lesión se generan unas sustancias conocidas con el nombre de prostaglandinas. Se las podría llamar también "mensajeros del dolor". Estas sustancias informan al sistema nervioso central de la agresión y se ponen en marcha los mecanismos biológicos de la inflamación, el dolor o la fiebre. En 1971 el farmacólogo británico John Robert Vane demostró que el ácido acetilsalicílico actúa interrumpiendo estos mecanismos de producción de las prostaglandinas y tromboxanos.28 29 Así, gracias a la utilización de la aspirina, se restablece la temperatura normal del organismo y se alivia el dolor. La capacidad de la aspirina de suprimir la producción de prostaglandinas y tromboxanos se debe a la inactivación irreversible de la ciclooxigenasa (COX), enzima necesaria para la síntesis de esas moléculas proinflamatorias. La acción de la aspirina produce una acetilación (es decir, añade un grupo acetilo) en un residuo de serina del sitio activo de la COX.
[editar]Efectos
[editar]Efectos antiinflamatorios
La aspirina es un inhibidor no selectivo de ambas isoformas de la ciclooxigenasa, pero el salicilato, el producto metabólico normal de la aspirina en el cuerpo, es menos eficaz en la inhibición de ambas isoformas. Los salicilatos que no son acetilados pueden tener funciones en la eliminación de radicales del oxígeno. La aspirina inhibe irreversiblemente a la COX-1, modifica la actividad enzimática de la COX-2 e inhibe la agregación plaquetaria, no así las especies no acetiladas del salicilato.14 Por lo general, la COX-2 produce los prostanoides, la mayoría de los cuales son proinflamatorios. Al ser modificada por la aspirina, la COX-2 produce en cambio lipoxinas, que tienden a ser antiinflamatorias. Los AINEs más recientes se han desarrollado para inhibir la COX-2 solamente y así reducir los efectos secundarios gastrointestinales de la inhibición de la COX-1.16
La aspirina también interfiere con los mediadores químicos del sistema calicreína-cinina, por lo que inhibe la adherencia de los granulocitossobre la vasculatura que ha sido dañada, estabiliza los lisosomas evitando así la liberación de mediadores de la inflamación e inhibe laquimiotaxis de los leucocitos polimorfonucleares y macrófagos.14
[editar]Efectos analgésicos
La aspirina es más eficaz reduciendo el dolor leve o de moderada intensidad por medio de sus efectos sobre la inflamación y porque es probable que pueda inhibir los estímulos del dolor a nivel cerebral subcortical. Es un ácido orgánico débil que tiene al mismo tiempo una función de ácido carboxílico y de fenol ya que también se le considera el orto fenol del acido benzoico (su nombre es ortofenometiloico). Tiene características antiinflamatorias pero debido a que provoca irritaciones estomacales no se aplica como tal sino en forma de sus derivados, siendo los más conocidos el ácido acetilsalicílico ("Aspirina") y el salicilato de metilo (el éster con el alcohol metílico).
[editar]Efectos antipiréticos
La aspirina reduce la fiebre, mientras que su administración sólo afecta ligeramente a la temperatura normal del cuerpo. Los efectos antipiréticos de la aspirina probablemente están mediados tanto por la inhibición de la COX en el sistema nervioso central como por la inhibición de la interleucina-1,14 liberada por los macrófagos durante los episodios de inflamación.
Se ha demostrado que la aspirina interrumpe la fosforilación oxidativa en las mitocondrias de los cartílagos y del hígado al difundir al espacio que está entre las dos membranas de la mitocondria y actuar como transportador de los protones requeridos en los procesos de la respiración celular.30 Con la administración de dosis elevadas de aspirina se observa la aparición de fiebre debido al calor liberado por lacadena de transporte de electrones que se encuentra en la membrana interna de las mitocondrias, contrariamente a la acción antipirética de la aspirina a dosis terapéuticas. Además, la aspirina induce la formación de radicales de óxido nítrico (NO) en el cuerpo, lo cual reduce la adhesión de los leucocitos, uno de los pasos importantes en la respuesta inmune a infecciones, aunque aún no hay evidencias concluyentes de que la aspirina sea capaz de combatir una infección.31 Datos publicados recientemente sugieren que el ácido salicílico y otros derivados de la aspirina modulan sus acciones de señalización celular por medio del NF-κB,32 un complejo de factores de transcripción que juegan un papel importante en muchos procesos biológicos, incluida la inflamación.
[editar]Efectos antiplaquetarios
Las dosis bajas de aspirina, de 81 mg diarios, producen una leve prolongación en el tiempo de sangrado, que se duplica si la administración de la aspirina continúa durante una semana. El cambio se debe a la inhibición irreversible de la COX de las plaquetas, por lo que se mantiene durante toda la vida de las mismas (entre 8 y 10 días).14 Esa propiedad anticoagulante hace que la aspirina sea útil en la reducción de la incidencia de infartos en algunos pacientes.33 40 mg de aspirina al día son suficientes para inhibir una proporción adecuada de tromboxano A2, sin que tenga efecto inhibitorio sobre la síntesis de prostaglandina I2, por lo que se requerirán mayores dosis para surtir efectos antiinflamatorios.34
En el año 2008 un ensayo demostró que la aspirina no reduce el riesgo de aparición de un primer ataque cardiaco o accidente cerebrovascular, sino que reduce el riesgo de un segundo evento para quienes ya han sufrido un ataque cardiaco o un accidente cerebrovascular. En mujeres que toman dosis bajas de aspirina cada dos días se disminuye el riesgo de un accidente cerebrovascular, pero no es un tratamiento que pueda alterar sustancialmente el riesgo de un infarto o muerte cardiovascular.35 En general, para un paciente que no tiene enfermedad cardíaca, el riesgo de sangrado supera cualquier beneficio de la aspirina.36
[editar]Interacciones
Artículo principal: Interacción farmacológica
El ácido acetilsalicílico ha sido profusamente estudiado lo que, añadido a su antigüedad, nos ha dado un amplio conocimiento de las interacciones con otros fármacos. Debido a la gravedad de los posibles efectos adversos como consecuencia de estas interacciones, hay que tenerlas muy presentes a la hora de su prescripción. Las más importantes están recogidas en las siguientes tablas, realizadas en función de los mecanismos de producción de las interacciones.
| Fármaco | Resultados de la interacción. |
|---|---|
| • Antiinflamatorios no esteroideos (AINE) | Puede incrementar el riesgo de úlceras y de hemorragias gastrointestinales, debido a un efecto sinérgico. |
| • Corticoides | Puede incrementar el riesgo de úlceras y de hemorragias gastrointestinales, debido a un efecto sinérgico. |
| • Diuréticos | La administración conjunta puede ocasionar un fallo renal agudo, especialmente en pacientes deshidratados. En caso de que se administren de forma simultánea ácido acetilsalicílico y un diurético, es preciso asegurar una hidratación correcta del paciente y monitorizar la función renal al iniciar el tratamiento. |
| • Inhibidores selectivos de la recaptación de serotonina (ISRS) | Aumenta el riesgo de hemorragia en general y de hemorragia digestiva alta en particular. |
| • Anticoagulantes orales | Aumenta el riesgo de hemorragia, por lo que no se recomienda. Si resulta imposible evitar una asociación de este tipo, se requiere una monitorización cuidadosa del INR. |
| • Trombolíticos y antiagregantes plaquetarios | Aumenta el riesgo de hemorragia. |
| Ejercen un efecto sinérgico en la reducción de la filtración glomerular, que puede ser exacerbado en caso de alteración de la función renal. La administración a pacientes ancianos o deshidratados, puede llevar a un fallo renal agudo por acción directa sobre la filtración glomerular. Además, pueden reducir el efecto antihipertensivo, debido a la inhibición de prostaglandinascon efecto vasodilatador. |
| • β-bloqueantes | Disminución del efecto antihipertensivo debido a una inhibición de las prostaglandinas con efecto vasodilatador. |
| • Insulina ysulfonilureas | Aumenta el efecto hipoglucemiante. |
| • Ciclosporina | Aumenta la nefrotoxicidad de la ciclosporina debido a efectos mediados por las prostaglandinas renales. |
| • Vancomicina | Aumenta el riesgo de ototoxicidad de la vancomicina. |
| • Interferón α | Disminuye la actividad del interferón-α. |
| • Alcohol | Aumenta el riesgo de hemorragia digestiva. |
Las interacciones farmacocinéticas van a cubrir prácticamente todo el espectro de posibilidades en cuanto al mecanismo de producción, aunque se muestran como más interesantes las de origen metabólico. En este sentido, parece ser independiente de la CYP3A4 y, al igual que otros AINE, estar ligada a la CYP2C9. No obstante, su abundante metabolismo al margen del hígado, hace que no sean fundamentales sus interacciones a nivel del citocromo P450. Las más interesantes se muestran en la siguiente tabla:
| Fármaco | Resultados de la interacción |
|---|---|
| • Metotrexato | Disminuyen la secreción tubular de metotrexato incrementando las concentraciones plasmáticas del mismo y por tanto su toxicidad. |
| • Litio | Disminuyen la excreción de litio, aumentando los niveles de litio en sangre, que pueden alcanzar valores tóxicos. |
| •Uricosúricos | Disminución del efecto uricosúrico y una disminución de la excreción del ácido acetilsalicilico alcanzándose niveles plasmáticos más altos. |
| • Antiácidos | Pueden aumentar la excreción renal de los salicilatos por alcalinización de la orina. |
| • Digoxina | Incremento de los niveles plasmáticos de digoxina que pueden alcanzar valores tóxicos. |
| •Barbitúricos | Aumenta las concentraciones plasmáticas de los barbitúricos. |
| • Zidovudina | Aumenta las concentraciones plasmáticas de zidovudina al inhibir de forma competitiva la glucuronidación o directamente inhibiendo el metabolismo microsomal hepático. |
| • Ácido valproico | Disminución de la unión a proteínas plasmáticas y una inhibición del metabolismo de ácido valproico. |
| • Fenitoína | Incremento de los niveles plasmáticos de fenitoína. |
Finalmente, la siguiente tabla muestra las interacciones no farmacológicas, manifestadas como alteraciones de los resultados de las pruebas de laboratorio:
| Resultados de la interacción. | Determinaciones analíticas afectadas. |
|---|---|
| Aumento biológico. | •fosfatasa alcalina •transaminasas (ALT y AST). •amoníaco •bilirrubina •colesterol •creatinquinasa •creatinina •digoxina •tiroxina libre •lactato deshidrogenasa (LDH) •globulina de unión a la tiroxina •triglicéridos •ácido úrico •ácido valproico |
| Reducción biológica | • Estriol (orina) •tiroxina libre •glucosa •fenitoína •TSH •TSH-RH •tiroxina •triglicéridos •triiodotironina •ácido úrico •aclaramiento de creatinina |
| Aumento analítico | •glucosa •paracetamol •proteínas totales |
| Reducción analítica | •transaminasas (ALT) •albúmina •fosfatasa alcalina •colesterol •creatina kinasa •lactato deshidrogenasa (LDH) •proteínas totales •ácido 5-hidroxiindolacético (orina) •ácido 4-hidroxi-3-metoxi-mandélico (orina) •estrógenos totales (orina) •glucosa (orina) |
| Nota: El aumento biológico consiste en un "verdadero aumento" del valor determinado, como consecuencia de la interacción con el organismo. El aumento analítico viene dado por una "falsa elevación" del valor determinado, como consecuencia de la interacción con los reactivos que forman parte de la técnica que determina los niveles de cada uno de ellos. De forma análoga ocurre con las reduccciones biológica y analítica. | |
En pacientes con cardiopatías establecidas, el ibuprofeno puede interferir con los efectos cardioprotectores de la aspirina cuando se administran ambos medicamentos al mismo tiempo.38
[editar]Uso clínico
- Dolor leve y moderado de origen variados, como el dolor de cabeza, períodos menstruales, resfríos, dolor en los dientes y dolores musculares.22 Sin embargo, no es efectiva para el dolor visceral severo. La aspirina y otros antiinflamatorios no esteroideos (AINES) se han combinado con analgésicos opioides para el tratamiento del dolor causado por el cáncer, donde los efectos antiinflamatorios actúan sinergísticamente con los opioides para aumentar la analgesia. La combinación de aspirina con oxicodona —una clase de analgésicos narcóticos— se usa para aliviar desde el dolor moderado al moderadamente intenso.39
- Enfermedad de Kawasaki, especialmente a dosis elevadas durante la fase febril.40
- Fiebre reumática, sobre todo la artritis reumatoide.
- Enfermedades autoinmunes tipo lupus eritematoso.22
- Otros trastornos inflamatorios de las articulaciones.
[editar]Protección cardiovascular
La aspirina disminuye la incidencia de ataques isquémicos, la angina inestable,trombosis de una arteria coronaria con infarto agudo de miocardio y la trombosis secundaria a un bypass coronario.22
[editar]Otros usos
Ciertos estudios epidemiológicos sugieren que el uso a largo plazo de la aspirina a bajas dosis se asocia con una reducción en la incidencia del cáncer colorrectal,41 42 43 44 así como el cáncer de pulmón,45 46 posiblemente por su asociación con efectos inhibitorios sobre la COX producida por adenocarcinomas,47 efectos supresores de prostaglandinas48 o incluso efectos directamente antimutagénicos.49 También se ha estudiado el papel que juega la aspirina en reducir la incidencia de otras formas de cáncer. En varios estudios se demostró que la aspirina no reduce la aparición del cáncer de próstata.50 51 Sus efectos en la prevención del cáncer de páncreas son mixtos, un estudio de2004 encontró un aumento estadísticamente importante en el riesgo de contraer cáncer pancreático en mujeres que tomaban aspirina,52mientras que un metaanálisis de varios estudios publicado en 2006 no encontró evidencias concluyentes de que la aspirina u otros AINEsestuvieran asociados a un riesgo aumentado de esta forma de cáncer.53 Es posible que la aspirina también tenga efectos positivos sobre el cáncer del tracto digestivo superior, pero las evidencias siguen aún siendo inconclusas.54 55
Se ha hipotetizado que la aspirina es capaz de reducir la formación de cataratas en pacientes diabéticos, aunque en al menos un estudio se demostró que no es eficaz en esa acción.56
[editar]Dosificación
Las dosis óptimas para alcanzar los efectos analgésicos o antipiréticos de la aspirina son menores de 0,6 a 0,65 gramos por vía oral. Dosis más elevadas pueden prolongar el efecto. La dosis habitual suele ser repetida cada 4 horas. La dosis antiinflamatoria en niños es de 50–75 mg por cada kg de peso del niño cada día dividida en varias dosis durante el día. La dosis de entrada promedio para un adulto es de 45 mg/kg/día en dosis divididas.
[editar]Efectos adversos
Artículo principal: Reacción adversa a medicamento
A las dosis habituales, los efectos adversos más comunes de la aspirina son la irritación gástrica, náuseas, vómitos, úlcera gástrica o duodenal,22 mientras que la hepatotoxicidad, asma, cambios en la piel y nefrotoxicidad son menos frecuentes. Se ha reportado que ocurre adaptación de la mucosa en pacientes con úlceras asociadas a la administración de aspirina de modo que se ha demostrado el mejoramiento espontáneo con el tiempo sin descontinuar la toma de la aspirina.14
Su ingesta abusiva produce nefritis, que son los procesos inflamatorios y/o disfuncionales del riñón y vasodilatación periférica por acción directa sobre el músculo liso. A dosis altas algunos pacientes han reportado vómitos, acúfenos, disminución de la audición, delirio, psicosis,estupor y vértigo los cuales son reversibles al reducir la dosis. A dosis aún mayores de salicilatos aparece una respiración profusa y comaresultado de un efecto directo sobre el bulbo raquídeo.14 A niveles tóxicos de salicilatos se presenta alcalosis respiratoria seguida deacidosis metabólica por acumulación del salicilato, depresión respiratoria, cardiotoxicidad e intolerancia a la glucosa. Dos gramos o aún menos de aspirina al día pueden aumentar los niveles de ácido úrico en sangre, mientras que las dosis que sobrepasan los 4 gramos diarios disminuyen los uratos. Igual que el resto de los AINEs, la aspirina puede causar una elevación en las enzimas hepáticas, hepatitis, disfunción renal, sangrado y asma.
[editar]Sangrado
Algunas personas se ven menos afectadas que otras por el efecto antiplaquetario de la aspirina. Un estudio ha sugerido que las mujeres son más resistentes a los efectos plaquetarios de la aspirina que los hombres57 58 y en otro estudio, cerca de un 30% de los pacientes evaluados eran así de resistentes a la acción secundaria de la aspirina.59
En ciertas ocasiones, puede aparecer un ligero sangrado gastrointestinal, por lo general causado por una gastritis erosiva que, con el tiempo, puede producir una deficiencia de hierro. En su forma comercial, no se debe administrar en niños menores de 12 años que padezcangripe o varicela (por lo general se usa paracetamol en vez) y/o usar en conjunto con otros salicilatos, ya que puede conducir al Síndrome de Reye, enfermedad rara, pero muy grave.4 La administración de aspirina durante un cuadro de dengue no se recomienda por razón de un aumento en el riesgo de hemorragias.60
La administración de aspirina en madres antes del parto puede causar trastornos hemostásicos en recién nacidos, incluyendo petequias,hematuria, cefalohematoma, hemorragia conjuntival y sangrado durante o después de una circuncisión. Por su parte, las madres pueden presentar con sangrado confinado al período intraparto o puerperio. Por ello, la administración de aspirina debe ser evitada durante elembarazo y si se sospecha que la madre ha tomado aspirina en los cinco días antes del parto, el recién nacido debe ser evaluado para descartar sangrados.61
Respecto a otras reacciones adversas (RAM), y a modo de resumen, se incluye una tabla siguiendo los criterios de la CIOSM.
| Sistema implicado | Grupo CIOSM. | Tipo de reacción |
| Aparato digestivo | Frecuentes | Úlcera gástrica, úlcera duodenal, hemorragia gastrointestinal (melenas,hematemesis), dolor abdominal, dispepsia, náuseas, vómitos. |
| Poco frecuentes | Hepatitis | |
| Aparato respiratorio | Frecuentes | Espasmo bronquial paroxístico, disnea grave, rinitis. |
| Piel y tejido subcutáneo | Frecuentes | Urticaria, erupciones cutáneas, angioedema. |
| Poco frecuentes | Sudoración | |
| Sangre y sistema linfático | Frecuentes | Hipoprotrombinemia |
| Sistema nervioso | Poco frecuentes | Mareos, confusión, tinnitus, sordera |
| Genitourinario | Raros | Insuficiencia renal y nefritis intersticial aguda |
| Otros | Poco frecuentes | Síndrome de Reye, cefalea. |
| Raros | Reacciones anafilácticas o anafilactoides | |
De forma global, puede afirmarse que entre el 5% y el 7% de los pacientes experimenta algún tipo de efecto adverso.37
[editar]Sobredosis
Tomar más de 150 mg/kg de aspirina puede provocar resultados graves e incluso mortales si no se recibe tratamiento. Para un adulto pequeño, eso equivale aproximadamente a tomar 20 tabletas que contienen 325 mg de aspirina. Los niños pueden resultar afectados con niveles mucho más bajos.62
Los pacientes con una sobredosis accidental o intencional de aspirina son sometidos a un lavado gástrico con carbón activado y se instala una producción abundante de orina alcalina. De presentar trastornos como hipertermia o desequilibrios en los electrolitos, deben ser restablecidos.14 En las intoxicaciones severas, puede que sea necesaria la hemodiálisis o, rara vez, la ventilación asistida. A menudo se emplean infusiones de bicarbonato de sodio para alcalinizar la orina conllevando a un aumento en el salicilato excretado fuera del cuerpo.62
[editar]Contraindicaciones
La acción antiplaquetaria de la aspirina hace que esté contraindicada en pacientes con hemofilia.63 Aunque en el pasado no se recomendaba el uso de la aspirina durante el embarazo, la aspirina puede tener utilidad en el tratamiento de la preeclampsia y aún en laeclampsia.14
La aspirina no debe administrarse en personas con antecedentes alérgicos al ibuprofeno o al naproxeno,64 65 o quienes sean de alguna forma intolerantes a los salicilatos66 67 o a los AINEs y se debe ejercer moderación en la prescripción de aspirina a pacientes asmáticos o con broncoespasmo inducida por los AINEs. Por motivo de su acción sobre la mucosa estomacal, se recomienda que los pacientes con enfermedad renal, úlceras pépticas, diabetes, gota o gastritis consulten con un profesional de la salud antes de tomar aspirina.64 63 Aún en la ausencia de estas enfermedades, siempre existe el riesgo de sangrado gastrointestinal cuando se combina la aspirina con el licor o lawarfarina.64 65
Se ha demostrado que la aspirina puede causar anemia hemolítica en pacientes con deficiencia de glucosa-6-fosfato deshidrogenasa(G6PD), en especial a grandes dosis y dependiente de la severidad de la enfermedad.68 69
[editar]Presentaciones
Respecto a las dosis, habitualmente las más bajas (300 mg o menos) se suelen utilizar como antiagregante plaquetario, ya que su uso en niños se ha restringido mucho. Las más elevadas se utilizan buscando el efecto analgésico/antipirético o el antirreumático. Respecto a las presentaciones se puede decir que prácticamente se han estudiado todas las posibles formas galénicas para el uso clínico del ácido acetilsalicílico. Las que a continuación se describen son las más comúnmente utilizadas:
- Comprimidos de 25 mg, 100 mg, 125 mg, 250 mg, 300 mg, 500 mg, 650 mg
- Comprimidos masticables de 500 mg
- Comprimidos efervescentes de 500 mg
- Comprimidos recubiertos de 100 mg y 300 mg
- Granulado efervescente, sobres de 500 mg
- Cápsulas (asociado a otros fármacos) para presentación retardada
- También podemos encontrarlo en dosificaciones inusuales, como la de 267 mg, asociado a otras sustancias.
Igualmente, existen multitud de presentaciones con otros fármacos asociados, habitualmente para el tratamiento de procesos catarrales. Es el caso de las asociaciones con fenilefrina, clorfenamina, cafeína, vitamina C (ácido ascórbico levógiro) o sustancias del complejo vitamínico B. Otras veces se asocia a otros fármacos para aumentar su efecto antiagregante (dipiridamol), o analgésico (paracetamol).
Respecto a los excipientes habituales se da una situación parecida. Tanto la forma galénica como las características organolépticas del fármaco obligan al uso de determinado tipos de excipientes. Sin embargo, el gran número de laboratorios que lo fabrican como fármaco genérico hace que los excipientes que podamos encontrarnos sean sumamente variables. No obstante a continuación se listan los que se suelen incluir en la forma comercial Aspirina (probablemente la más vendida en el mundo) y algunos de los más usuales en las formas genéricas:
Artículo principal: Números E
- Colorantes:
- Conservantes y antioxidantes:
- ácido ascórbico (E-200),
- Citratos: ácido cítrico anhidro (E-330), citrato de sodio (E-331)
- Estabilizantes y emulgentes:
- Celulosa en polvo (E-460 II)
- Estearato de calcio, (E-470 A)
- Reguladores del pH y antiaglutinantes:
- Carbonatos: carbonato de sodio (E-500), Hidrogenocarbonato de sodio (E-500 I), carbonato de magnesio pesado (E-504)
- Otros:
- Edulcorantes, como el aspartamo (E-951), el manitol (E-421) o el almidón de maíz, (gelificante y espesante)
- Aromatizantes muy variables, entre ellos el aroma de zumo de mandarina, aroma de naranja o aroma seco especial,
- Carmelosa de sodio, celulosa microcristalina.
- Los comprimidos recubiertos suelen llevar en la capa externa copolímero de ácido metacrílico tipo C, dodecilsulfato de sodio (E-514), polisorbato 80, talco o citrato de trietilo (E-1505).
Suscribirse a:
Entradas (Atom)




